泽璟制药斑秃治疗新药获批临床 然核心氘代药物研发未来或难打破原研专利
《科创板日报》(上海,记者 徐红)讯,国家药监局网站显示,由苏州泽璟生物制药股份有限公司开发的盐酸杰克替尼乳膏近日获批临床,拟开发适应症为轻中度斑秃和轻中度特应性皮炎。这也是继辉瑞(Pfizer)的PF-06651600片之后,国内第二款获批临床的斑秃治疗新药。
辉瑞PF-06651600片是一款口服酸激酶(JAK3)抑制剂,于今年3月在国内获批临床,适应症为用于治疗≥12岁中重度斑秃患者(包括全秃[AT]和普秃[AU])。
脱发问题日益受到社会关注。日前,央视财经有报道称,近年来我国脱发人群呈直线上升趋势,平均6个人中就有1人脱发,我国脱发的人群已经超过2.5亿。而作为全球发病率第二高的脱发症状,全球范围内大约有1.47亿斑秃患者,中国大约有400万。但与巨大患者人群不匹配的是,目前为止并没有治疗斑秃的通用疗法,FDA也没有批准任何治疗斑秃的药物。
首家以第五套标准申报科创板上市,核心产品多个适应症将陆续报产
6月10日,苏州泽璟生物制药股份有限公司(简称“泽璟制药”)的科创板上市申请获得上海证券交易所受理,成为第120家获得受理的企业,也是第一家以第五套上市标准进行申报的企业,即:预计市值不低于人民币40亿元,主要业务或产品需经国家有关部门批准,市场空间大,目前已取得阶段性成果。医药行业企业需至少有一项核心产品获准开展二期临床试验,其他符合科创板定位的企业需具备明显的技术优势并 满足相应条件。
目前,泽璟制药正处于问询阶段,并在7月31日发布了对上交所问询的第一轮回复。从公开资料看,交易所的问询主要集中在公司股权结构、主营业务、核心技术等方面。
据泽璟制药招股说明书,公司是一家专注于肿瘤、出血及血液疾病、肝胆疾病等多个疾病治疗领域的新药研发企业。依托精准小分子药物研发及产业化平台、复杂重组蛋白生物新药研发及产业化平台这两大新药创制核心技术平台,公司同时进行化学小分子新药和重组蛋白质大分子新药的研发和生产。
目前,公司产品管线包括11个创新药物的23项在研项目,其中甲苯磺酸多纳非尼片、外用重组人凝血酶及盐酸杰克替尼片的多种适应症已分别处于 II/III 期临床试验阶段;奥卡替尼及注射用重组人促甲状腺激素处于I期临床试验阶段;盐酸杰克替尼乳膏则刚获批临床,盐酸杰克替尼片治疗自身免疫相关疾病和ZG5266处于IND申请的准备阶段;此外,小分子新药ZG0588 及ZG170607、抗肿瘤双靶点抗体新药ZG005及ZG006 处于临床前研发阶段。
已进入临床试验阶段的产品概要如下表所示:
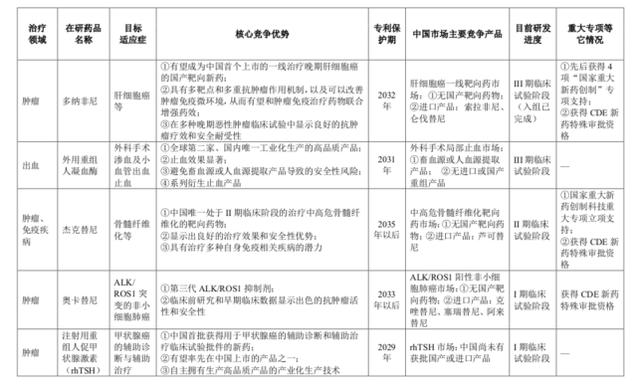
(来源:公司招股说明书)
公司预计, 将于2019年下半年提交多纳非尼一线治疗晚期肝细胞癌的上市申请,2020年将完成多纳非尼三线治疗晚期结直肠癌的III期临床试验并依据III期临床试验结果提交NDA申请(新药上市申请),2021年将完成多纳非尼治疗局部晚期/转移性放射性碘难治性分化型甲状腺癌和外用重组人凝血酶用于治疗外科手术渗血止血的III期临床试验并提交NDA申请。
氘代药物研发:未来专利壁垒突破难度或加大
泽璟制药也被认为是继Concert与Auspex(2015年被仿制药巨头TEVA收购)之后的全球第三大氘代药物公司。氘代药物亦可叫做重药、重氢药或含氘药,就是把药物分子上处于特定代谢部位的一个或多个碳氢键(CH)用碳氘键(C D)替代所获得的药物。同非氘代母药相比,氘代药物具备疗效可能更优、药代性质更佳、给药频率降低及不良反应发生率更低等优势。
自2008年至今,已上市氘代药物有一个,另有多个处于临床Ⅲ期研究。Auspex与Concert共同开发的氘代药物—氘代丁苯那嗪(商品名:Austedo)于2017年4月获FDA批准,是世界上首个氘代药物。在国内市场上,除了泽璟制药以外,成都海创药业有限公司、泰基鸿诺、正大天晴等企业也都有布局氘代药物。
在泽璟制药的现有产品管线中,多纳非尼、杰克替尼、奥卡替尼均属于氘代产品,对应的氘代原研药分别是索拉非尼(拜耳)、JAK抑制剂Momelotinib(吉利德)和EGFR T790M抑制剂奥希替尼(阿斯利康)。
虽然近年来氘代药物引起了制药行业越来越多的关注,成为新药研发的一种捷径,但市场对其的未来研发前景也存在一定隐忧。
“近些年,很多国际制药企业包括辉瑞、诺华、默克、阿斯利康、罗氏、礼来及百时美施贵宝等都开始采用氘代技术来研发新药,其优点是药物研发风险低,成药性高,但未来氘代药会很难做,因为原研对专利的保护会越来越严格,专利突破会很难。”一位一级市场投资人对记者表示。
