「观察」寻生物药企涨幅逻辑,静待再鼎医药的商业化拐点

(来源:再鼎医药)
再鼎医药未来是不是生物科技领域的明星难以解答,但是眼下,由于短期涨幅巨大,明星一词并不过分。自2020年9月28日于港交所上市交易以来,截至2021年1月21日收盘,再鼎医药股价录得149.83%涨幅。
如此的涨幅或许来源于三个方面:管理层运营策略、与创投机构的联系、即将商业化的产品。
再鼎通过与GSK、BMS、Paratek、Five Prime、Entasis、Novocure、MacroGenics、Deciphera、Incyte、Regeneron及Turning Point建立合作伙伴关系,在中国、香港、澳门以及(在若干情况下)台湾、澳大利亚、新西兰及亚太地区其他国家拥有12个活跃的引进授权临床候选药物可供开发。
于2015年3月,再鼎与百时美施贵宝签订了授权协议,据此再鼎获独家授权在中国、香港及澳门开发、制造、使用、出售、进口及商业化brivanib,并附带独家权利在若干条件下将授权区域扩展至包括台湾及韩国。根据该协议,再鼎需向百时美施贵宝支付按brivanib销售净额计得的里程碑付款及特许权费。
而观察杜莹(再鼎创始人)博士的履历,除了光鲜的药企研发背景以外,在创办再鼎医药之前,其曾于红杉资本中国基金任职两年。此外,启明创投亦持有再鼎较大的股份。
简之,上述策略叠加与资本市场密切的联系,可为后续其余潜在企业投资机会作为一项评价标准。
以上,便是再鼎医药重要的投资背景。
再鼎医药
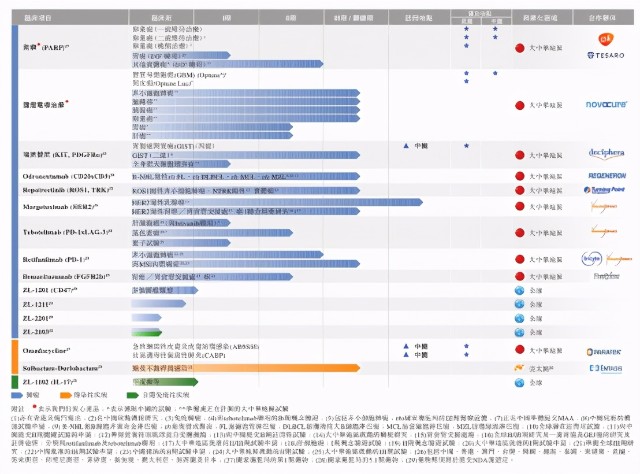
(再鼎医药产品布局 来源:再鼎医药)
策略玩的再好,还需要具体的产品作为底层支撑。目前,再鼎的核心看点在于三项产品:则乐、optune(脑肿瘤电场治疗)、瑞派替尼。
则乐(尼拉帕利)为每日一次的小分子聚(ADP-核糖)聚合酶1/2或PARP 1/2抑制剂,获国家药监局批准成为中国治疗多种实体瘤类型的1类药物。则乐分别于2017年3月获FDA及于2017年11月获EMA批准,用作复发性铂敏感型卵巢癌女性患者的维持治疗。该维持治疗用于该等先前接受治疗但预期癌症会复发的女性患者,旨在避免或减缓先前治疗缓解后癌症的复发。铂敏感型癌症为一种经最初铂类化疗后会缓解及化疗后缓解期超过六个月的疾病。
香港卫生署于2018年10月批准则乐,再鼎于2018年12月在香港推出则乐。于2019年6月,则乐获得上市许可,可于澳门将则乐商业化,用于治疗复发性卵巢癌女性患者。中国国家药品监督管理局(或国家药监局)于2019年12月批准则乐用于对铂类化疗有完全或部分缓解的复发性上皮性卵巢癌、输卵管癌或原发性腹膜癌成人患者的维持治疗,随后再鼎于2020年1月于中国推出则乐。
截至2020年8月31日,则乐已在中国一个省及六个城市成功获纳入与中国基本医疗保险计划互补的区域性报销计划。截至2020年8月31日,则乐亦获列入市政府所指导的17种商业健康保险及12种补充保险。
竞争上,截至2020年7月,中国仅有两种上市的PARP抑制剂,一种为于2018年获批来自阿斯利康的利普卓(奥拉帕尼);另一种为于2019年获批的则乐(尼拉帕利)。
阿斯利康的利普卓于2018年12月获FDA批准用于一线维持治疗,但仅适用于BReast CAncer基因(「BRCA」)阳性患者;其次于2020年5月获FDA批准用于同源重组缺乏症(HRD)阳性的癌症患者,其占晚期卵巢癌患者中的50%,但仅可与阿瓦斯汀(贝伐单抗)联用。相比之下,则乐获批用于所有晚期卵巢癌患者,而不论其生物标志物状态,并且可以作为单药疗法。
另外四种PARP抑制剂正在中国进行III期临床开发或处于NDA阶段,包括在中国及全球开发的候选药物。其中三种PARP抑制剂的主要适应症专注于晚期卵巢癌,而另一种则侧重转移性前列腺癌。在晚期卵巢癌适应症中,其中一种产品仅针对BRCA阳性患者。
Optune(肿瘤电场治疗)为一种便携式电池或电源供电设备,其通过电绝缘表面换能器数组向患者剃光头发的头部传递低强度(1-3 V/cm)及中频(100-300 kHz)的交替肿瘤电场治疗而产生作用。
肿瘤电场治疗为一种癌症疗法,即使用调节至特定频率的电场来阻断细胞分裂,抑制肿瘤生长并导致受影响癌细胞死亡。Optune已获FDA根据上市前批准申请(「PMA」)批准与化疗药物TMZ联用治疗新诊断为GBM(胶质母细胞瘤)的成人患者,并批准用于治疗在接受化疗作为单一疗法后确诊复发GBM的成人患者。Optune亦获批准或已获发CE证书以将Optune在欧盟、日本及若干其他国家上市用于治疗GBM。
于2018年9月,再鼎与Novocure进行全球战略发展合作,据此,再鼎获得在中国、香港及澳门开发及商业化Optune(肿瘤电场治疗)的独家授权。于2019年8月,国家药监局就Optune授予创新医疗器械认定;于2020年5月,国家药监局批准了Optune的上市许可申请(MAA),且毋须进行与TMZ联用治疗GBM新患者的临床试验,且亦可用作治疗复发性GBM患者的单一疗法,使Optune自2007年以来成为中国首个获批的胶质母细胞瘤疗法。于2020年8月,Optune Lua TM 在香港推出用于治疗MPM获得Optune的独家授权到在香港上市。
于2020年6月在中国推出Optune起,Optune获列入省政府或市政府所指导的4种补充保险。
瑞派替尼为一种处于临床开发阶段的研究性KIT及PDGFRα激酶开关调控抑制剂,用于治疗KIT及╱或PDGFRα驱动的癌症,包括GIST、系统性肥大细胞增多症(或SM)以及其他癌症。瑞派替尼特别设计用于通过抑制KIT及PDGFRα的广谱突变来改善GIST患者的治疗。
瑞派替尼为一种KIT及PDGFRα抑制剂,可阻断GIST中涉及的第9、11、13、14、17及18外显子中的初始及继发性KIT突变以及SM中涉及的原发性D816V第17外显子突变。瑞派替尼还抑制GIST的一个亚群中涉及的第12、14及18外显子中的原发性PDGFRα突变,包括第18外显子D842V突变。
再鼎于2019年6月自Deciphera获得在中国、香港、澳门及台湾开发及商业化瑞派替尼的独家授权。
总结
总体而言,相较于其他生物科技企业,再鼎布局的产品(大部分来自授权)均临近商业化阶段,但由于潜在的市场空间并不确定,因此倘若未来商业化盈利难以匹配市值表现,其股价短期或有下跌的风险,投资者应当做好风险平衡。
作者:周治玮
